
14/1/2019 - Nota de prensa
Nota realizada por la Universidad de Princeton
Un reciente estudio liderado por la Universidad de Princeton, en el que ha participado Toni Celià-Terrassa, actualmente investigador del grupo de investigación en Terapia Molecular del Cáncer del IMIM, ha conseguido reducir la propagación del cáncer de mama triple negativo en ratones mediante la proteína Tinagl1.
El agente terapéutico Tinagl1 está basado en una proteína de origen natural y bloquea dos de las principales vías mediante las que las células del cáncer de mama pueden crecer y migrar fuera del tumor primario para propagarse hacia otros órganos del cuerpo. El estudio se ha publicado en la revista Cancer Cell.
«Otras investigaciones han intentado bloquear la propagación de esta forma de cáncer pero todos los intentos hasta ahora han fracasado debido a que cuando se aborda un enfoque, las células cancerosas lo compensan encontrando otra vía de escape», afirmó Yibin Kang, profesor de Biología Molecular de Warner-Lambert / Parke-Davis en la Universidad de Princeton. «Con este nuevo enfoque, el tratamiento bloquea ambas vías al mismo tiempo. Es como matar dos pájaros de un tiro.»
El cáncer de mama triple negativo es un tipo de cáncer muy agresivo que representa entre el 12 y el 17 por ciento de todos los casos de cáncer de mama. Su nombre responde a la ausencia de tres importantes dianas biológicas - el receptor de estrógeno (ER), el receptor de progesterona (PR) y el receptor del factor de crecimiento epidérmico humano 2 (HER2) - que se utilizan para localizar y eliminar las células cancerosas.
Las pacientes con cáncer de mama triple negativo presentan mayores índices de recurrencia después de la quimioterapia, además de la carencia de dianas moleculares efectivas. Esto se traduce en un pronóstico general más desfavorable. Los nuevos hallazgos sugieren que la proteína recombinante Tinagl1 es un candidato idóneo para seguir investigando para desarrollar un nuevo tratamiento para este tipo de cáncer.
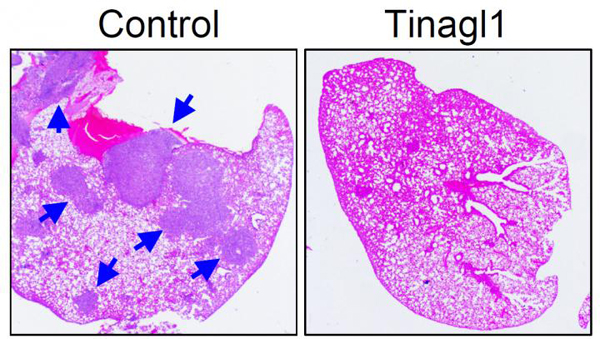
Imagen: el tratamiento con proteína tinagl1 recombinante suprimió significativamente la metástasis pulmonar, como muestran las flechas azules en las imágenes correspondientes a ratones con (derecha) y sin (izquierda) tratamiento con tinagl1. Créditos: imagen cortesía de Yibin Kang y col., Universidad de Princeton
Los investigadores observaron que la Tinagl1 inhibe las dos vías principales que contribuyen a la agresividad y la resistencia a los tratamientos del cáncer de mama triple negativo. La Tinagl1 inhibe cada una de las dos vías de un modo diferente, anulando los mecanismos de compensación que el cáncer utiliza para escapar a los tratamientos.
La Tinagl1 combate el cáncer mediante la inactivación de una proteína que promueve la formación de tumores, conocida como receptor del factor de crecimiento epidérmico (EGFR). Las mutaciones en este gen causan una amplificación de la actividad de señalización del EGFR, el cual envía señales que inducen la proliferación celular y estimulan el crecimiento tumoral y la metástasis a otras zonas del cuerpo. Los tratamientos dirigidos al EGFR han demostrado escasa relevancia clínica, posiblemente debido a que las células cancerosas encuentran vías de crecimiento alternativas.
Esta proteína también actúa sobre unas moléculas denominadas integrinas que participan en la regulación de la migración celular hacia nuevas localizaciones, la unión con otras células y la transformación en tumores. Parece que la Tinagl1 es capaz de actuar sobre la señalización de las integrinas al interferir con una proteína relacionada denominada quinasa de adhesión focal (FAK), que promueve la migración, el crecimiento y la supervivencia celulares.
Según explican los responsables de la investigación, ambas vías están interconectadas a nivel molecular, creando redundancias y compensaciones que contribuyen a la agresividad y la resistencia a los tratamientos del cáncer de mama triple negativo.
Los investigadores examinaron cerca de 800 muestras de tumores de mama procedentes de pacientes humanos. Observaron que las muestras con menor expresión del gen Tinagl1 procedían con mayor probabilidad de pacientes con tumores en fase avanzada y tiempos de supervivencia cortos. Los tumores con mayores niveles de expresión de este gen estaban más fuertemente vinculados a resultados positivos para el paciente.
La diferencia era más notable dentro del subgrupo de los cánceres de mama triple negativo.
Para comprobar si la presencia del gen Tinagl1 podía proteger frente al crecimiento y la propagación tumoral, los investigadores crearon células tumorales de humanos y de ratones con altos niveles de expresión de este gen. Observaron que una expresión elevada del gen Tinagl1 en células cancerosas de ratones producía tumores de crecimiento más lento y menos propensos a la metástasis pulmonar.
Los investigadores también administraron proteína Tinagl1 a ratones con tumores de mama y observaron que el tratamiento de siete semanas inhibía notablemente el crecimiento del tumor primario y la metástasis pulmonar espontánea, además de no presentar efectos secundarios significativos. En un estudio para conocer la cronología del tratamiento con Tinagl1 se comprobó que este compuesto era eficaz incluso después de que el tumor hubiera empezado a metastatizar. El equipo también estudió el mecanismo de supresión de la Tinagl1 y observó que esta proteína inhibe las vías de señalización tanto del EGFR como de la integrina/FAK, proporcionando así resultados mejores que al utilizar inhibidores independientes para cada una de las vías.
El estudio ha sido dirigido por el primer autor Minhong Shen, investigador posdoctoral asociado; junto con los coautores de la Universidad de Princeton Yong Wei, profesional especialista asociado; Brian Ell, exalumno de posgrado; Xinlei Sheng, alumno de posgrado; Mark Esposito, investigador posdoctoral asociado; Jooeun Kang, exinvestigador universitario, clase de 2014; Xiang Hang, investigador especialista; Hanqiu Zheng, becario posdoctoral; Michelle Rowicki, estudiante universitaria, clase de 2020; Toni Celia-Terrassa, investigador postdoctoral asociado; Ileana Cristea, profesora de biología molecular; y Yibin Kang. También han contribuido al estudio Yi-Zhou Jiang, Yirong Liu y Zhi-Ming Shao, del Centro para el Cáncer de la Universidad de Fudan en Shanghái; Weichung Shih, del Instituto de Cáncer Rutgers de Nueva Jersey; y Lanjing Zhang, del Centro Médico Universitario de Princeton.
El estudio ha sido financiado por la Fundación Brewster, el Departamento de Defensa de Estados Unidos, Susan G. Komen y la Comisión para la Investigación sobre el Cáncer de Nueva Jersey.
Estudio de referencia:
"Tinagl1 suppresses triple-negative breast cancer progression and metastasis by simultaneously inhibiting integrin/FAK and EGFR signaling ". Se publicó en la revista Cancer Cell de 3 de enero de 2019.
© Institut Hospital del Mar
d'Investigacions MèdiquesAviso legal y Política de Privacidad | Política de cookies | Mapa Web | Accesibilidad | Dirección y accesos | Contacto